肌腱作為連接肌肉與骨骼的關鍵組織,具有細胞密度低、血供差的生理特點,損傷后自愈能力極弱,易形成瘢痕組織并伴隨術后黏連、慢性炎癥及感染等問題,最終導致肌腱力學性能下降、關節功能障礙,轉變為難治性疾病。目前臨床常用的肌腱修復手段以手術縫合為主,輔以傳統支架材料,但這類材料存在明顯短板:一是靜態性能難以匹配肌腱動態愈合的階段性需求,肌腱在炎癥期、增殖期和重塑期對力學支撐與生物信號調控的需求差異顯著,傳統材料難以實現精準的階段化適配;二是缺乏有效的抗黏連與抗感染設計,術后周圍組織黏連是影響肌腱功能恢復的主要因素,而臨床常用抗菌手段易破壞局部免疫微環境;三是外源性電刺激需依賴外部電源,生物電信號雖為調控肌腱細胞遷移與膠原合成的關鍵因素,但傳統電療設備的有創性及便攜性限制使其臨床應用受阻。
近期,蘭州大學口腔醫學院范增杰教授團隊提出“仿生梯度+動態適配”的設計理念,開發出一種集自供電壓電刺激、仿生抗黏連與多梯度時空調控于一體的3D打印復合支架,從材料設計、結構構筑和功能調控三個層面系統解決肌腱修復的核心難題。該支架制備所使用模板由摩方精密microArch? S230(精度:2 μm)3D打印設備加工而成。相關研究成果以“A 3D-Printed Piezoelectric Scaffold With Bio-Inspired Gradient and Dynamic Adaptation for Tendon Regeneration”為題發表在國際知名學術期刊《Advanced Materials》上。蘭州大學口腔醫學院碩士研究生黃欣悅為第一作者,蘭州大學口腔醫學院范增杰教授為獨立通訊作者。
本研究的核心設計亮點在于構建了一種兼具荷葉仿生抗黏連結構及力學、壓電、降解三梯度的復合支架(圖1)。通過微納3D打印與疏水改性,支架外層構筑超疏水物理屏障以抗成纖維細胞黏附,內層保持親水以促進干細胞再生,實現“外抗內促”的雙向調控。通過調控PHBV濃度,支架在縱向上形成了力學梯度與壓電梯度,使中層在愈合早期提供強電刺激以抗炎,后期隨內外層降解暴露低強度電刺激以引導膠原定向重塑,從而實現無需電源的自供電動態調控。同時,支架降解速率遵循由內向外遞減的規律,實現支架降解與組織再生的時空同步。此外,本研究通過優化水/DMF/DCM溶劑體系,解決了疏水PHBV與親水SA/PAM水凝膠的相容性問題,為精準打印均相穩定的功能梯度并協同滿足肌腱動態愈合需求奠定了材料基礎。
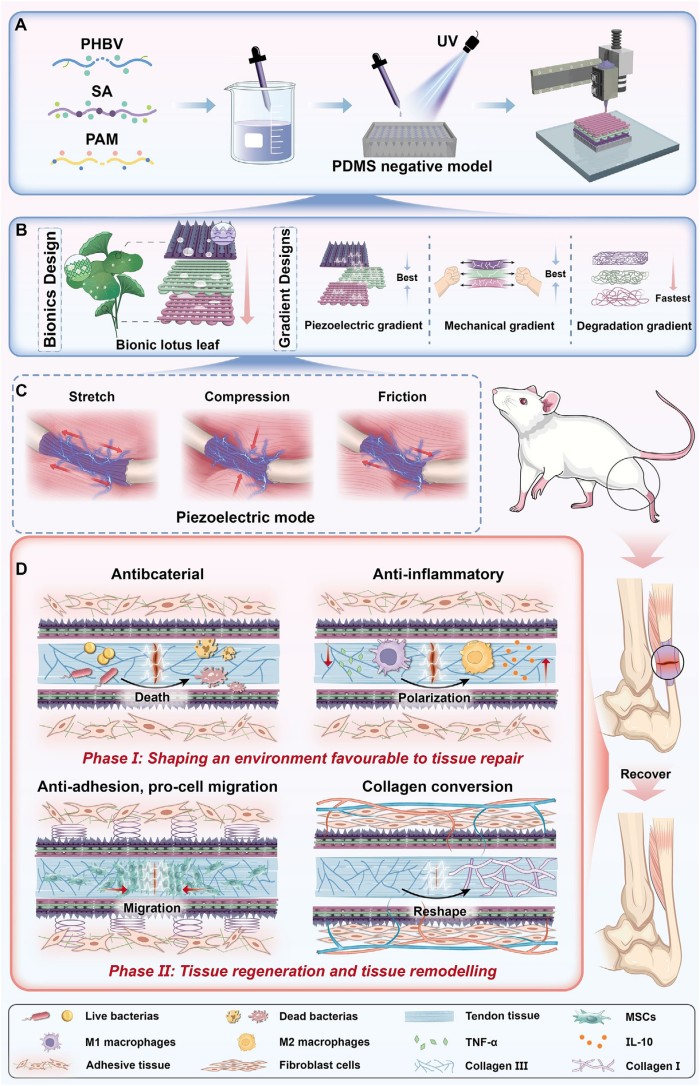
圖1.研究示意圖。
使用摩方精密microArch? S230(精度:2 μm)制備荷葉表界面仿生陣列的陽模,并通過PDMS翻模獲得陰模,進而制備3D打印復合支架。掃描電鏡(SEM)與能譜分析(EDS)結果顯示,支架各層孔徑和元素分布均勻,荷葉仿生微結構成型精準,為支架的體內外性能發揮提供了可靠的結構保障。同時,支架的壓電輸出可隨肌腱生理應變動態調控,在拉伸、壓縮和摩擦三種生理運動模式下均能穩定產電;水含量與溶脹率隨PHBV濃度梯度變化,外層低溶脹率保證了抗黏連性能,內層高溶脹率有利于營養物質運輸;28天降解實驗顯示,支架降解率隨PHBV濃度升高而降低,實現了從快到慢的梯度降解,精準匹配肌腱愈合的時間進程(圖2)。
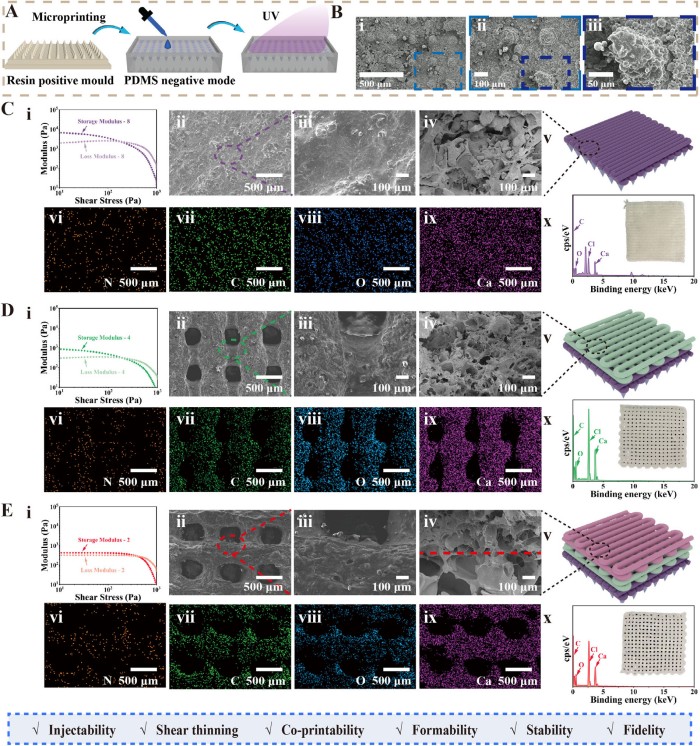
圖2.復合支架的設計、打印。
進一步對支架的理化性能進行系統表征,驗證了其作為肌腱修復材料的可行性。支架的壓電輸出可隨1%-5%的生理應變動態調控,在拉伸、壓縮和摩擦模式下均能穩定產電;其溶脹率與降解速率隨PHBV濃度梯度呈現由內向外遞減的規律,既保證了外層抗黏連結構的穩定,又為內層營養物質運輸和組織長入提供了充足空間。
本研究還系統評估了復合支架的體外肌腱修復效果。生物相容性評估顯示,支架浸提液無細胞毒性,并能促進BMSCs增殖,溶血率低于5%;大鼠皮下植入實驗進一步證實其可有效調控炎癥反應并引導膠原有序重塑。此外,支架展現出廣譜抗菌活性,對大腸桿菌和金黃色葡萄球菌的抑制率分別達100%和99%以上,對MRSA及銅綠假單胞菌亦有顯著抑制效果,其壓電效應介導的物理抗菌機制有效避免了抗生素耐藥風險。細胞骨架染色、劃痕實驗與EdU檢測表明,支架的壓電刺激可促進BMSCs的伸長、遷移與增殖,細胞鋪展面積與增殖率顯著高于對照組;qRT-PCR結果顯示,支架可顯著上調肌腱特異性標志物(Tnmd、Scx、Tnc)的表達,同時下調促炎因子TNF-α、IL-6的表達,上調抗炎因子IL-10的表達,促進RAW264.7細胞向M2型巨噬細胞極化,營造有利于肌腱再生的抗炎微環境。
復合支架的體內肌腱修復效果在大鼠跟腱3 mm缺損模型中得到了系統驗證。術后1周與3周的大體觀察顯示,復合支架組(tGS)肌腱周圍無明顯黏連組織,而對照組與無壓電成分支架組(nGS)存在嚴重的纖維組織黏連;H&E與Masson染色結果表明,tGS組缺損區域被新生組織完全填充,膠原纖維呈波浪狀定向排列,與天然肌腱結構高度相似,而對照組膠原纖維排列紊亂,瘢痕組織大量形成。步態分析與生物力學測試進一步驗證了支架的功能修復效果:術后3周,tGS組大鼠跟腱的運動功能指數(AFI)顯著優于其他組,爪印長度、寬度與正常側無顯著差異;生物力學測試顯示,tGS組修復肌腱的彈性模量、最大拉伸應力等指標與天然肌腱接近,力學性能得到有效恢復。免疫組化染色結果表明,復合支架組的組織重塑效果最佳,同時炎癥水平最低。
最后,通過轉錄組測序與機器學習分析揭示了該支架促進肌腱再生的深層分子機制。術后3周,tGS組共鑒定出1376個差異表達基因,其中機械轉導、膠原生物合成等再生相關通路顯著上調,而炎癥激活與氧化應激通路被抑制。在分子層面,支架通過阻斷IKKβ/NF-κB、p38MAPK及JAK-STAT等關鍵炎癥信號通路,有效下調促炎因子表達,并誘導M2型巨噬細胞極化,極化指數達3.70倍;其疏水外層則通過抑制ERK1/2信號通路,從源頭減少成纖維細胞的異常增殖與遷移,進而防止術后黏連。機器學習分析進一步證實,該支架能夠選擇性激活所有M2亞型并抑制M1經典亞型,從而構建穩定的抗炎再生微環境,最終在基因表達層面協同促進膠原重塑與肌腱功能恢復。
綜上所述,該3D打印復合支架的核心創新在于將仿生結構與力學、壓電、降解和潤濕性多梯度調控一體化集成,首次實現了自供電動態電刺激、階段化力學支撐、時空可控降解與雙向生物界面的協同匹配。以PHBV/SA/PAM為材料體系,該支架通過精準3D打印解決了傳統修復中靜態性能與動態愈合脫節、黏連與感染難以兼顧、外源性干預存在創傷等瓶頸問題。體內外實驗證實,其可有效調控炎癥微環境、抑制術后黏連并促進肌腱特異性再生;轉錄組與機器學習進一步揭示了其通過多信號通路協同調控再生的分子機制。該研究為肌腱修復提供了新范式,也為軟組織再生工程提供了重要的設計策略。
原文鏈接:https://doi.org/10.1002/adma.202517298











